藥企144張GMP證書被收回 中藥飲片佔82張
- 發佈時間:2015-12-30 09:38:03 來源:廣州日報 責任編輯:吳起龍
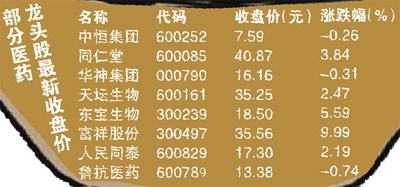
中藥企業是“重災區” 比例遠超化學藥企 相關企業或被淘汰出局
日前,《2015年全國收回藥品GMP證書情況統計》出爐,今年全國共有140家藥企144張GMP證書被收回。記者了解得知,中藥仍是“重災區”,今年被取消GMP證書的飲片企業成為“主流”。廣東某連鎖藥房負責人向本報透露,廣東存在數百家飲片企業,目前關門比例遠高於化學藥企,部分明知道不達標已放棄GMP要求,所以監管部門現場檢查基本一抓一個準。
觀察人士分析認為,我國醫藥行業仿製藥生産過剩、研發創新不夠,GMP大刀斬下無力改造、不符要求的藥企,促進行業洗牌加速。消費者不必擔心缺醫少藥,龍頭藥企則可能進一步提高市場集中度。
年中時本報曾報道新版GMP(藥品生産品質管理規範)大考難過,數十藥企淚別市場。日前,《2015年全國收回藥品GMP證書情況統計》出爐,今年全國共有140家藥企144張GMP證書被收回。
全年收回
82張中藥飲片GMP證書
中藥是收回證書“重災區”,今年被取消GMP證書的飲片企業成為“主流”。中藥飲片方面,今年全年收回82張證書,佔總收回數的56.9%;去年收回20張,佔去年總收回數的40%。記者獲悉,不少經營不佳、財力有限的藥企,不願再進行高投入改造,轉而通過出售等方式主動退出市場;而被收回證書者也損失慘重,很可能面臨市場丟失、經銷商解約等局面。
“廣東有數百家規模不一的飲片企業,很多都是歷史原因遺留下來的手工作坊轉變而成。就行業蒐集的資訊發現,目前越來越多飲片企業在加速消亡,雖然沒有具體數據,但公認其比例遠超過化學藥企。”對此,廣東某連鎖藥房負責人告訴記者,由於GMP參照的是歐美化學藥標準,所以國內稍有底氣的化學藥企,努力一把就能順利通關認證,相較之下,中藥和飲片企業總體在標準化、規範化、透明化方面落伍嚴重。“以前是缺乏標準化意識,現在是缺乏技術或資金。”他認為。
偏偏今年食藥監總局重點盯上了中藥飲片和中藥企業,事先不通知就實施快速現場檢查,一旦發現嚴重問題即可能收回GMP證書。對此有業內人士認為,今年估計將有超過10%的飲片企業失去生産資格甚至被沒收GMP證書。
重金屬
殘留量限度標準難過關
一位廣州中藥材經銷商告訴記者,今年以來“認栽”關門的飲片企業非常多,他們面對幾大現實難題。“新版GMP制定了中藥材及飲片中二氧化硫等重金屬殘留量限度標準,但小廠一般都從藥材市場低價收購原料,農民從種植源頭就沒能把關重金屬殘留,到了藥廠木已成舟,很可能過不了標準關;對很多小廠而言,如果要大力投入改造,各方面符合GMP要求,但又不能規模化量産,就會出現成本陡增、出廠價翻番、市場競爭力大幅削弱現象。所以小廠只能鋌而走險,直到不允許生産的那一天來臨。”該經銷商認為。
而記者了解得知,中藥飲片的原料問題仍是行業性“頑疾”,有的藥企被收回證書的原因就是發現原料霉變後還編造虛假檢驗結果。“所以大型藥企都在自建種植基地,從源頭把控品質和價格,避免被動局面。”他透露。
或因如此,藥市今年格外蕭條。“藥企對原料抓得越嚴,市場散收藥材的可能性就越低;倒下的一大批中藥企業也使得藥材成交量明顯減少;還有部分藥企採取觀望態度,減産過冬,農戶和經銷商今年日子都不好過。”某中藥分析師告訴記者。
業內分析
市場不會缺藥漲價
市場終端會否因為大批藥企下馬而感受到缺醫少藥、價格上漲?對此業內人士表示消費者可以放寬心。“基本上常見藥都有數十種同一配方不同品牌的産品在競爭,所以基本不會出現缺醫少藥現象,也沒有聽説由此導致終端價格上漲。”他表示,發改委放開藥價後,部分品類有不同程度漲價,但都屬於市場行為,基本與GMP證書收回無關。
而對於手握新版證書、市場屹立不倒的醫藥龍頭股而言,政策肅清行業風氣、促使洗牌加快,也可能助其提升市場集中度。“投資者在關注感興趣個股業績、産品佈局同時,也應了解其證書是否在手,目前就有個別上市公司主動透露還在完成改造爭取證書中。”該觀察人士表示。
新版GMP
被認為是規範藥企小亂散利器
GMP被業界認為是規範國內藥企小、亂、散狀況的利器。此前數據顯示,全國共有70.02%的企業通過新版GMP認證。但今年被收回GMP證書的藥企已遠超去年的81家。
按照新版GMP要求,所有藥品生産企業均應在今年底前達標,否則就會被淘汰出局,未在規定期限內通過認證的企業(車間),明年起不得繼續生産藥品;而收回GMP證書則尚有迴旋餘地,意味企業還可以“改過自新”,藥企暫停生産、按要求整改,經藥監部門再次核查確認達標後,可發回證書。
據了解,藥企要想生産藥物,必須手握生産許可證、藥品品種註冊證以及GMP認證。1998年我國參照國際標準首推GMP認證,對企業從廠房到設備、人員、衛生等生産環節提出要求,強調所有藥品不通過認證不得生産。此後2010年新版GMP認證落地,硬體部分參照歐盟標準,軟體部分參照美國藥監局標準,被稱為“史上最嚴認證”。








