水光針埋線熱瑪吉納入最高類醫械管理引發關注
發佈時間: 2022-04-08 16:09:28 | 來源: 中國網健康 | 責任編輯: 張豐
3月30日,國家藥品監督管理局經過將近半年廣泛徵集調整意見,出臺了《醫療器械分類目錄》部分醫療器械調整內容的公告。

據悉,本次調整是為進一步深化醫療器械審評審批制度改革,依據醫療器械産業發展和監管工作實際,按照《醫療器械監督管理條例》、《醫療器械分類目錄動態調整工作程式》的有關要求,對27類醫療器械內容進行調整,其中包括射頻治療(非消融)設備、整形美容用注射材料、整形用植入線材等産品類別。
我國對於醫療器械有著嚴格的分類,而三類醫療器械是最高級別的醫療器械。也就是説,目前大家常見的面部埋線項目,以玻尿酸、水光針等為代表的注射用透明質酸鈉溶液,以熱瑪吉、熱提拉、黃金微針為代表的射頻治療儀,均與人工心臟瓣膜、人工關節、血管支架等一樣,同屬於植入人體、對人體具有潛在危險,對其安全性、有效性必須嚴格控制的醫療器械。
調整公告公示後,立即引起社會廣泛關注,尤其涉及整形的産品全部被納入第三類管理類別,更是引起醫療美容行業的強烈反響。許多整形行業內的專家認為,這意味著處於行業上游的醫療器械領域正呈現加強監管的態勢,具體來看有三種變化:
第一,從無到最嚴。本次調整中,面部埋植線、面部提拉線在調整前是沒有被列入《醫療器械分類目錄》中,調整後直接被列入最高類。
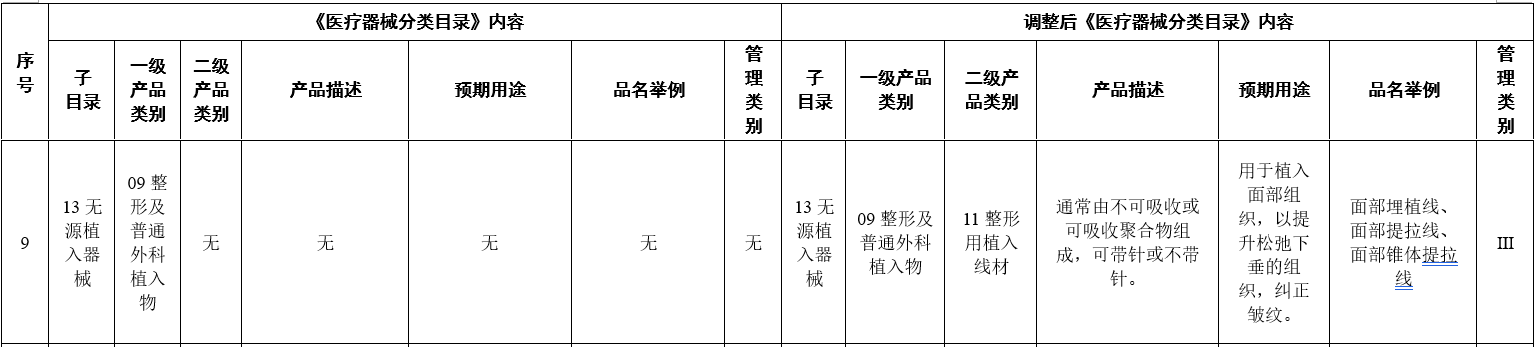
第二,從二類到三類。此次調整對風光無限的熱瑪吉,特別是爭議不斷的熱瑪吉五代做了界定。事實上,在2021年4月24日,國家藥品監督管理局就發佈了關於徵求《射頻美容類産品分類界定指導原則》(徵求意見稿),對於熱瑪吉五代的射頻美容類産品進行了界定。
射頻醫美項目的應用領域主要為抗衰老,屬於微創治療。治療前需要局部麻醉,手術過程中有痛感,術後面部會出現紅腫或少量結痂。截至2021年10月,通過國家藥品監督管理局認證的有21款,國內自主研發的射頻醫美器械僅有武漢中科科裏和德技醫療器械的2款器械。
值得注意的是,在去年11月公佈的徵求意見稿中,將用於面部、體部、頸部等非創傷性淺表治療的高頻電場皮膚熱治療儀、射頻治療儀,擬按照II類器械監管。正式調整後,均為第三類。
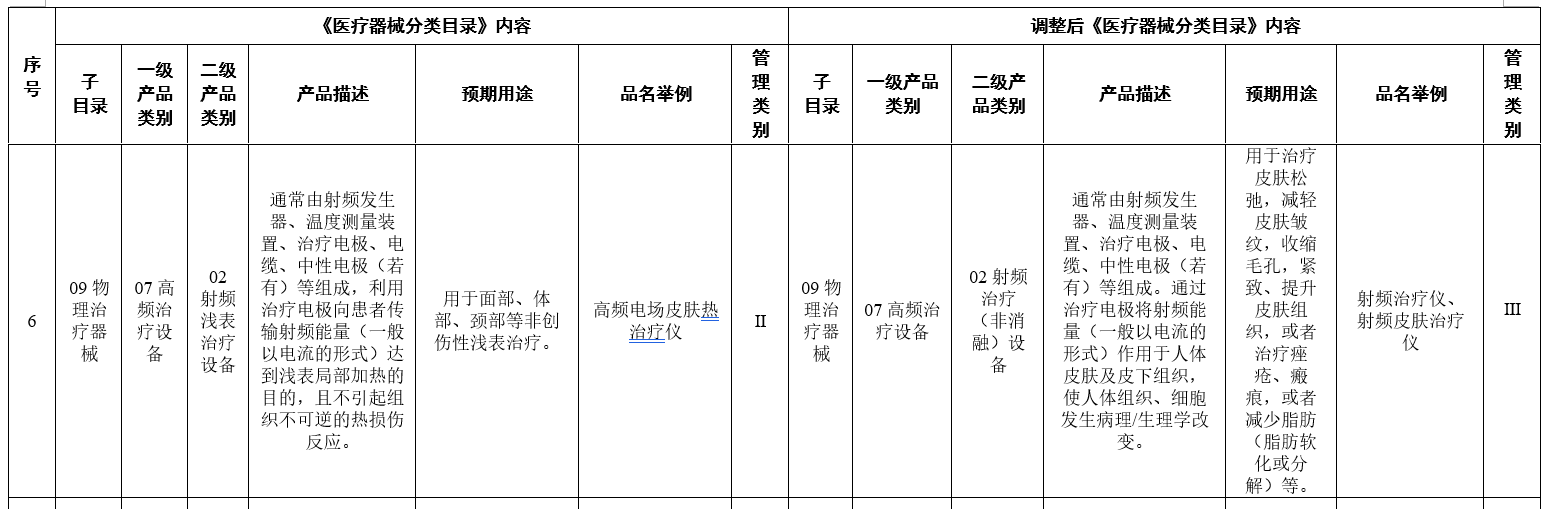
另外,留給射頻器械生産廠商、銷售商只有兩年的調整時間,2024年4月1日後,未取得醫療器械註冊證不得生産、進口和銷售。
第三,調整前就屬於三類器械的整形用注射填充物雖然級別不變,但是在産品描述、預期用途、品名舉例中,都做了內容調整。《目錄》顯示,注射用透明質酸鈉溶液,用於注射到真皮層,主要通過所含透明質酸鈉等材料的保濕、補水等作用,改善皮膚狀態,明確按照III類醫療器械監管。
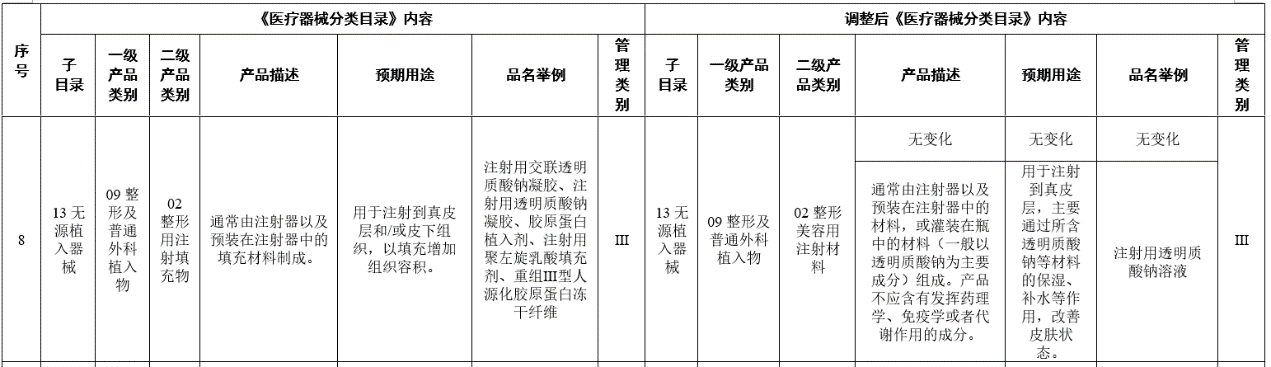
由此可以看出,此次調整對醫美器械管理賦予了積極意義,特別是針對無證照的非法黑醫美打擊力度更大。其一,説明皮膚修復、面部抗衰等醫美的網紅項目,相關診療辦法和醫療器械應用也逐漸成熟,以後不能再打擦邊球;其二,明確醫療屬性,明確射頻治療儀、面部埋植線及提拉線、注射用透明質酸鈉溶液屬於具有較高風險,需要採取特別措施嚴格控制管理以保證其安全、有效的醫療器械;其三,醫美行業上游廠商納入強監管,完善醫美全産業鏈監管範圍,為消費者提供全方位的安全保障。
值得注意的是,國家藥品監督管理局在公佈《醫療器械分類目錄》部分醫療器械內容的同一天,還刊登了全國市場監管部門廣告監管工作會議的報道。

會議以視頻形式召開,全面總結2021年廣告監管和指導廣告産業發展工作,分析了當前形勢,部署了2022年重點任務,要求持續強化廣告導向監管,著力規範和凈化廣告市場秩序。
《醫療美容廣告執法指南》第五條指出,市場監管部門依法整治各類醫療美容廣告亂象,著力解決危害性大、群眾反映集中的問題,對部分情形予以重點打擊,其中包括:宣傳診療效果或者對診療的安全性、功效做保證性承諾,對食品、保健食品、消毒産品、化粧品宣傳與醫療美容相關的疾病治療功能等。
從此次部分醫美器械調整內容來看,宏觀描述産品的預期用途裏,首次提到了“減輕皮膚皺紋,收縮毛孔,緊致、提升皮膚組織,保濕、補水……”等這些名詞。品名舉例也分別確定了“射頻治療儀、射頻皮膚治療儀、注射用透明質酸鈉溶液、面部埋植線、面部提拉線、面部錐體提拉線”。
我們知道,醫療器械的産品描述和預期用途,是對一類産品共性內容的基本描述,用於指導具體産品所屬類別的綜合判定,列舉的品名舉例為符合《醫療器械通用名稱命名規則》的規範性、代表性名稱。
此次預期用途和品名舉例的調整,明確各概念的定義及應包含的要素,有利於消費者了解預期用途是否與心理預期匹配,有益於在醫療器械監管中建立統一的認識,使監管工作更科學。
由此我們可以預判,調整後的醫美器械將在生産、銷售、使用、廣告宣傳上,迎來更全面更規範的相關行業大檢查。我們期待,能夠徹底清除擾亂行業秩序的黑醫美,讓喧囂、紛亂歸於寧靜規範,還醫美行業一片凈土。(淩燕)
